2025年7月11日,中国科学技术大学生命科学与医学部基础医学院、免疫应答与免疫治疗全国重点实验室田志刚教授、彭慧教授课题组与法国艾克斯-马赛大学Eric Vivier教授团队合作在《Science Immunology》期刊在线发表题为“Innate lymphoid cells originate from fetal liver–derived tissue-resident progenitors”的研究论文。该研究提出固有淋巴细胞(Innate lymphoid cell, ILC)胎肝起源模型,从时间和空间上解析了不依赖骨髓的ILC动态发育过程,重新定义ILC发育框架。
ILC是具有组织驻留特性的异质性群体(包含ILC1、ILC2和ILC3),对机体抵抗病原体、抗肿瘤及免疫调节等具有重要作用。传统观点认为,骨髓作为机体出生后的主要造血器官,是免疫细胞发育分化的关键场所。因此,研究人员长期以来主要在骨髓中寻找和鉴定ILC的前体细胞(ILC precursor, ILCP),然而,也有证据表明骨髓之外的组织中也有ILCP的存在。近年来,田志刚教授课题组发现肝脏驻留NK细胞(后续国际命名为ILC1)由肝脏原位造血前体细胞产生(Science 2021; J Exp Med 2022),提示ILC存在独立于骨髓造血的起源路径。
为进一步拓展上述发现,探究各外周组织驻留ILC亚群是否存在共性发育起源路径,研究人员构建了造血干细胞(HSC)谱系示踪模型(Fgd5 fate-mapping),可以标记示踪不同周龄小鼠造血干细胞的起源、发育和分化轨迹,发现骨髓造血来源的组织驻留ILC仅占15%-35%,而胚胎肝脏造血则可产生ILC的所有群体。研究人员利用单细胞测序和体内外分化体系,进一步解析了胎肝ILC共有祖细胞定向分化为特定ILC亚群前体细胞的发育轨迹,发现并鉴定了一群表达CD94的ILC前体,该前体具有ILC1和ILC3潜能,命名为ILC1/3P。在胚胎发育过程中,胎肝造血产生的ILCP迁移并定植于外周组织。随个体发生,组织微环境引导ILCP向ILC1/3P或ILC2P分化,最终形成具有显著组织区域特性的ILC亚群,该发育过程不依赖骨髓。即使在病原体感染或炎症状态下,局部组织ILC亚群大幅扩增,其来源依然独立于骨髓造血,提示成年组织ILCP具有自我更新和分化潜能。相比之下,骨髓主要产生经典NK细胞和部分骨髓内的ILC2。基于以上发现,这项研究揭示了骨髓并非ILC主要来源,ILC各细胞群体均起源于胚胎肝脏造血,从而提出了ILC共有起源、个体发生和发育分化的新模型,为后续研究ILC亚群在各器官的区域分化和功能特性奠定了基础。
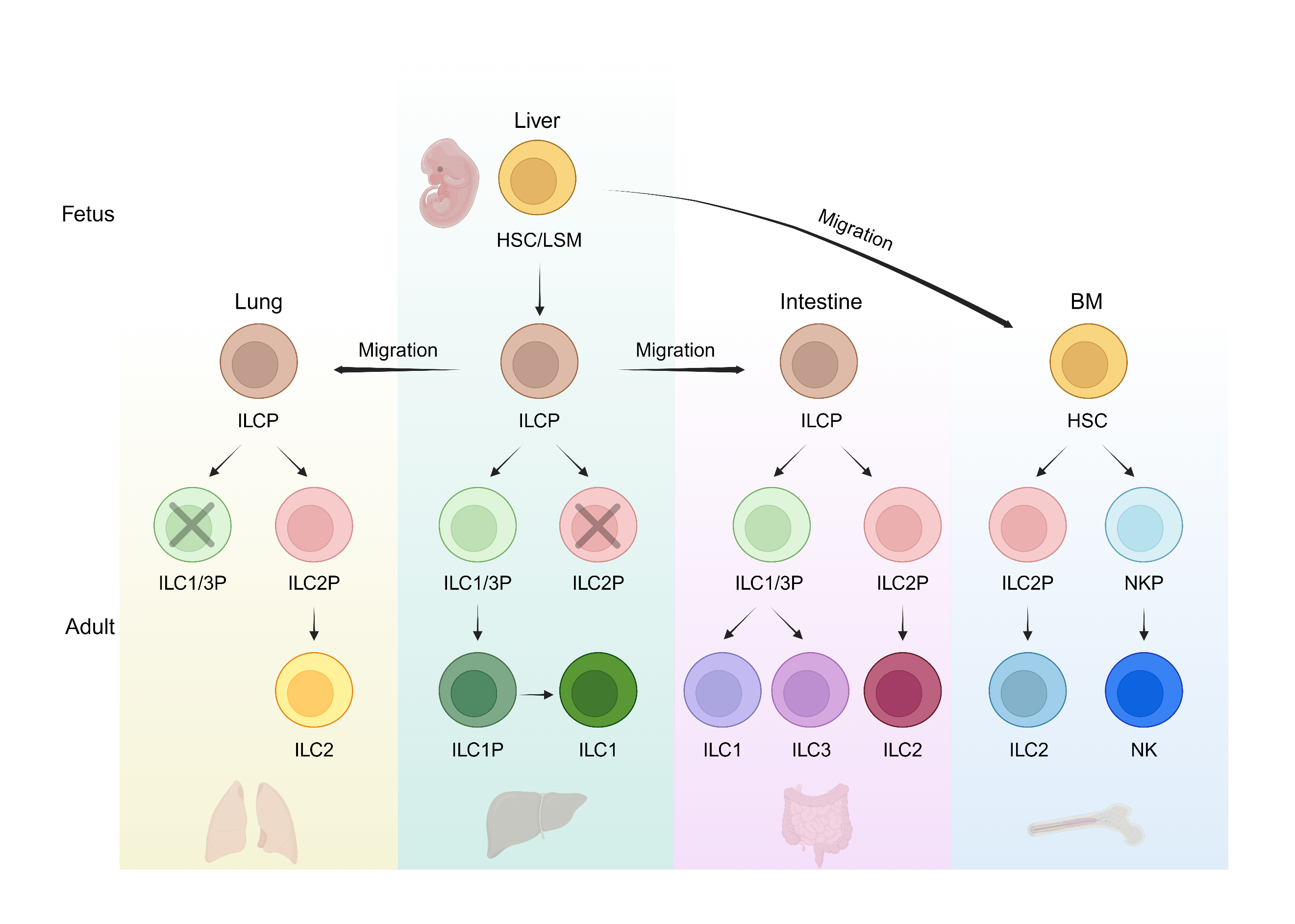
ILC胚胎起源和发育过程
中国科学技术大学免疫应答与免疫治疗全国重点实验室田志刚教授、彭慧教授和法国Eric Vivier教授为文章共同通讯作者,中国科学技术大学特任副研究员王宪伟、李佳瑞博士和法国Lucas Rebuffet博士为共同第一作者。该研究获得了山东大学张彩教授、陆军军医大学叶丽林教授、中国科大魏海明教授和朱书教授的帮助和支持,并受到国自然基金委、科技部、中科院以及合肥综合性国家科学中心大健康研究院等项目资助。
论文链接:https://www.science.org/doi/10.1126/sciimmunol.adu7962
