恒定自然杀伤T(invariant Natural Killer T cell,iNKT)细胞是CD1d限制的T淋巴细胞,具有固有免疫特性,表达半恒定T细胞受体(T Cell Receptor, TCR)。iNKT细胞除了直接或间接的抗肿瘤功能外,还具有低细胞毒性和异体移植安全等优势,所以iNKT细胞治疗具有广泛的应用前景。但肿瘤组织iNKT细胞功能异常和浸润能力低下是限制iNKT细胞发挥抗肿瘤功能的重要原因,所以对其机制的探索至关重要。目前,相关的调控机制研究主要从静态调控角度解析瘤内iNKT细胞激活前后状态与功能异常的关系,但瘤内iNKT细胞浸润和功能的动态调控机制尚不清楚。
2024年2月9日,中国科学技术大学生命科学与医学部白丽教授课题组在《Nature Communications》上在线发表了题为‘Motility and tumor infiltration are key aspects of invariant natural killer T cell anti-tumor function’的研究论文,揭示巨噬细胞和肿瘤VCAM1调控瘤内iNKT细胞运动和功能的相关机制。
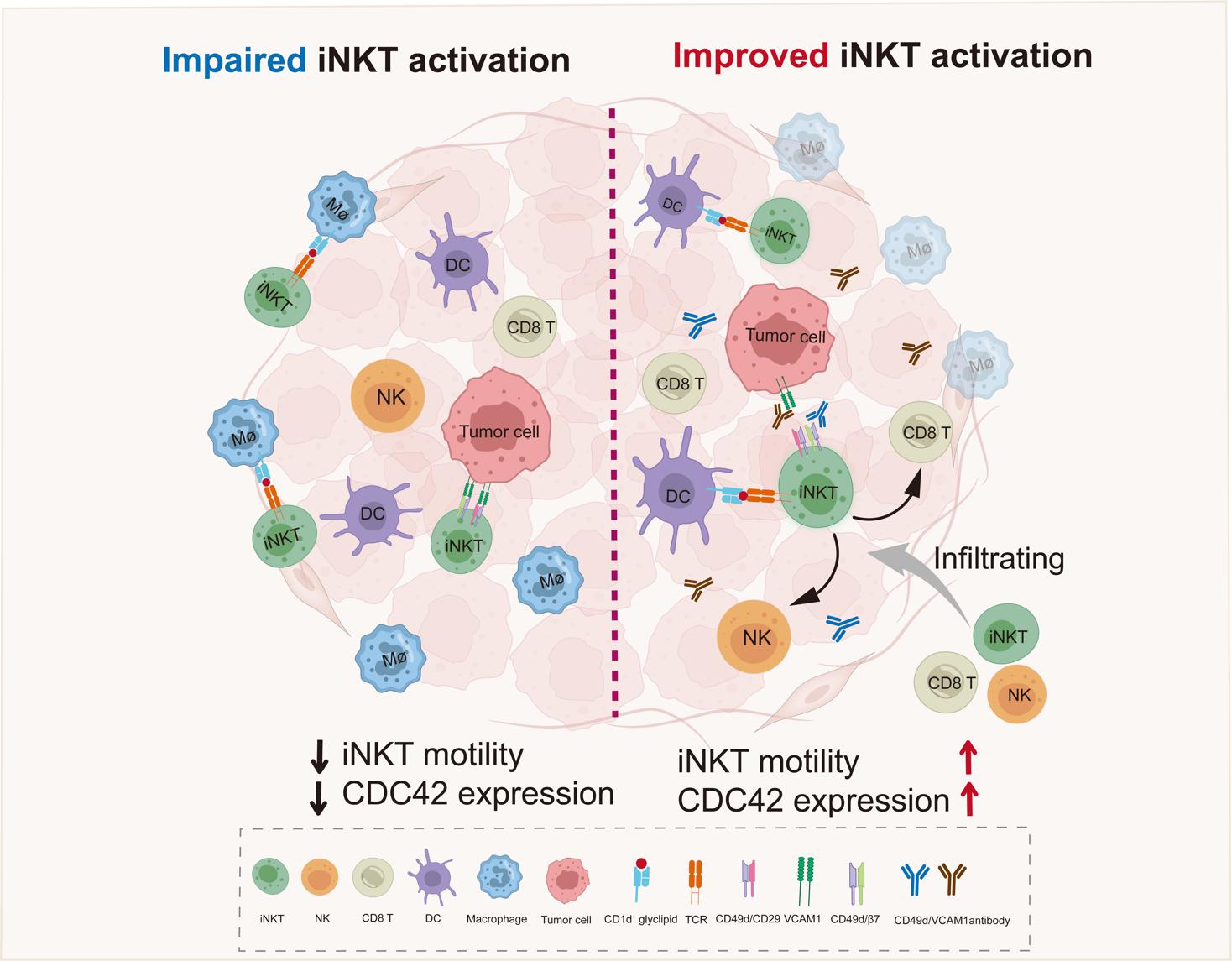
本研究通过多种肿瘤模型及活体成像技术发现肿瘤组织巨噬细胞通过CD1d分子与iNKT细胞相互作用,进而抑制iNKT细胞向肿瘤内部浸润并限制iNKT细胞与DC的互作,但巨噬细胞不影响瘤内iNKT细胞的运动。随后,本研究还发现肿瘤细胞通过VCAM1/CD49d抑制瘤内iNKT细胞CDC42表达,限制瘤内iNKT细胞运动,抑制瘤内iNKT细胞与DC互作进而抑制其激活。以上结果表明巨噬细胞和肿瘤VCAM1均可限制瘤内iNKT细胞激活过程进而加快肿瘤的生长进程。本研究还证实阻断VCAM1治疗及清除巨噬细胞可以促进瘤内iNKT细胞浸润并增强iNKT细胞介导的抗肿瘤效应,明显抑制了肿瘤的生长进程。
综上所述,本研究从动态调控角度解析了调控iNKT细胞免疫应答的分子机制,为提高iNKT细胞治疗效果提供了新的思路和策略。中国科学技术大学生医部博士研究生田晨曦为本文的第一作者,中国科学技术大学生医部白丽教授、张会敏副教授、傅思成特任副研究员为本文的共同通讯作者。本研究得到中国科学技术大学生医部王育才教授的大力帮助,该工作得到了微尺度国家研究中心和合肥综合性国家科学中心大健康研究院的大力支持,以及科技部、国家自然科学基金委和中国科学院等项目的资助。
原文链接:
https://www.nature.com/articles/s41467-024-45208-z
